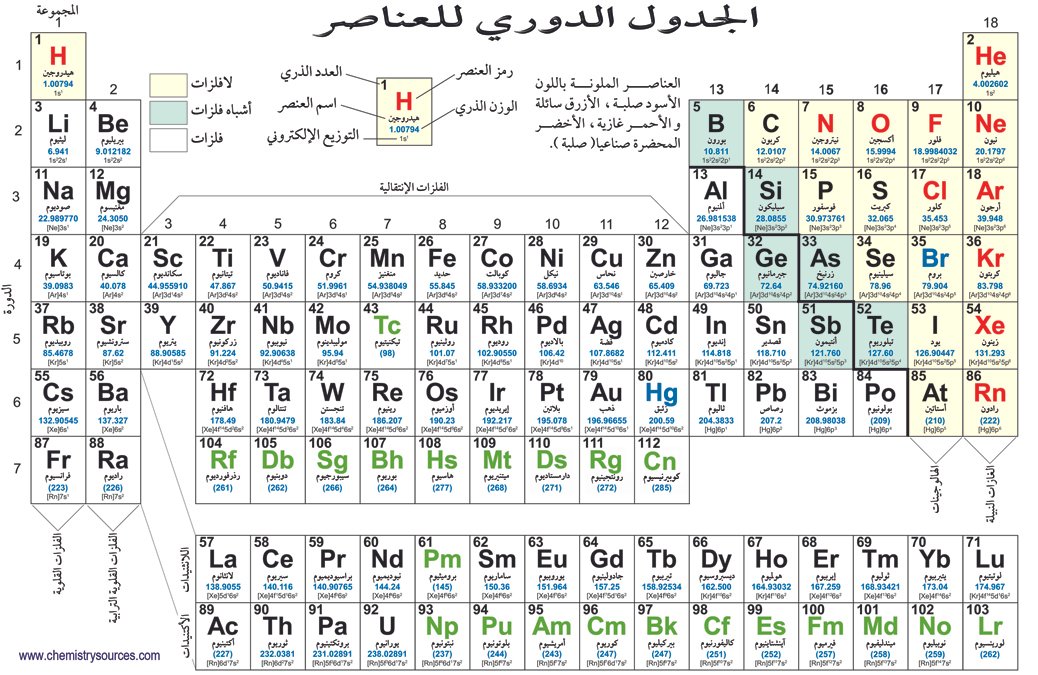
الفلزات
تعني العنصر الكيميائي الذي يفقد الالكترونات ليكوّن أيونات موجبة (كاتيونات) وتوجد رابطة فلزية بين ذراته،
كما يتم وصف الفلزات أيضاً على أنها شبكة من الأيونات الموجبة (كاتيونات) داخل سحابة من الالكترونات.
وتقع الفلزات في الثلاث مجموعات للعناصر التي تتميز بتأينها وخواصها، مع أشباه الفلزات واللا فلزات.
خواص الفلزات :
1- لها بريق معدني (لامعة). 2- جيدة التوصيل للحرارة والكهرباء.
3- قابلة للطرق والسحب. 4- درجة انصهارها عالية نسبياً.
5- ذات كثافة عالية.
ويرجع هذا بصفة عامة لكثافتها القليلة، وطراوتها، بينما الفلزات ذات درجة حرارة
الإنصهارالمنخفضة تكون نشيطة ونادرا ما يمكن تواجدها في حالتها العنصرية الفلزية.
أنواع الفلزات :
1- الفلزات النبيلة (المعادن الكريمة)
2- الفلزات القلوية منها (البوتاسيوم وهو شديد التفاعل مع الماء وعند حرقه يعطي لهبا ليلكيا).
3- فلزات الاتربة القلوية.
4- الفلزات الانتقالية.
5- الفلزات الرديئة.
أهمية الفلزات
تستخدم الفلزات في صناعة الكباري والحلي وأدوات الطهي والسيارات والمواد الفولاذية وغيرها.
اللافلزات
تتميز بخصائص معينة من ناحية التأين والترابط وتتبع وذلك لأنها عالية السالبية الكهربائية،
أي أنها تكتسب الكترونات التكافؤ من الذرات الأخرى أسرع من فقدها.
خواص اللافلزات :
1- ليس لها بريق معدني . 2- غير قابلة للطرق والسحب.
3- رديئة التوصيل للحرارة. 4- درجة انصهارها منخفضة نسبياً.
أنواع اللافلزات :
صلبة مثل : الكربون والكبريت والفسفور.
سائلة مثل : البروم.
الغازي مثل : الأكسجين والهيدروجين والكلور.
أهمية اللافلزات :
1- الأكسجين : إسعاف المرضى، وأسطوانات الغوص تحت الماء، وعمليات التلحيم.
2- الجرافيت : صنع الأقطاب الموجبة للأعمدة الجافة.
3- الأماس : صناعة الحلي.
(اليورانيوم والقنبلة النووية)
.. || ثقف نفسك .. موسوعة خُطَت بأيديكم .. منكم وإليكم #تفاعلي || ..
[ منتدى نور المعرفة ]
النتائج 1 إلى 20 من 48
مشاهدة المواضيع
-
6-1-2015 01:27 AM #33



- تاريخ التسجيل
- Mar 2009
- المـشـــاركــات
- 8,025
- الــــدولــــــــة
- سوريا
- الــجـــــنــــــس
- أنثى
الـتـــقـــــيـيــم:









 مجموع الاوسمة: 39
مجموع الاوسمة: 39 رد: .. || ثقف نفسك .. موسوعة خُطَت بأيديكم .. منكم وإليكم #تفاعلي || ..
رد: .. || ثقف نفسك .. موسوعة خُطَت بأيديكم .. منكم وإليكم #تفاعلي || ..
Loading...





 رد مع اقتباس
رد مع اقتباس

المفضلات